Yazar:
Lewis Jackson
Yaratılış Tarihi:
6 Mayıs Ayı 2021
Güncelleme Tarihi:
1 Temmuz 2024

İçerik
Ortalama kütle atomu, bir atomun kütlesinin doğrudan ölçüsü değildir. Bunun yerine, bu, elementin tipik bir örneğinden gelen atom başına ortalama kütledir. Milyarlarca tekil atomun kütlelerini ölçebiliyorsanız, ortalamalarını hesaplayarak bunu öğrenebilirsiniz. Kimyasal elementin farklı izotopları hakkındaki bilgilere dayanan daha pratik bir yöntemimiz var.
Adımlar
Bölüm 1/2: Ortalama kütle atomunu hesaplayın
İzotopları ve kütle atomlarını anlayın. Doğada, çoğu element birçok formda veya izotopta bulunur. Aynı elementin iki izotopu arasındaki tek fark, nötron sayısı kütle atomunu etkileyen atomdaki nötronların sayısıdır. Ortalama kütle atomunu hesaplamak, bu farkın etkisini hesaba katar ve size bu atomların bir örneğindeki her bir atomun ortalama kütlesini söyler.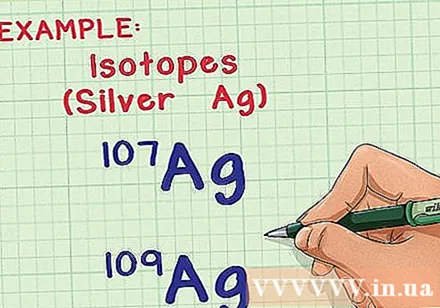
- Örneğin, gümüş (Ag) elementinin iki doğal izotopu vardır: Ag-107 ve Ag-109 (veya Ag ve Ag). İzotop, "kütle numarası" ndan veya bir atomdaki proton sayısı ile nötron sayısının toplamından sonra adlandırılır. Bu, Ag-109'un Ag-107'den iki daha fazla nötron içerdiği anlamına gelir, yani atomu biraz daha ağırdır.
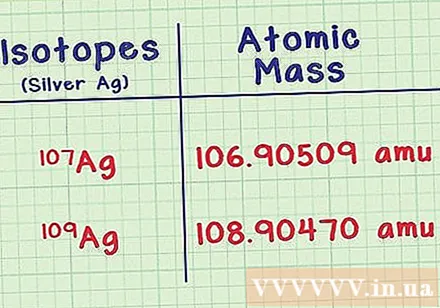
Her izotopun kütlesini bulun. Her izotop için iki parça bilgiye ihtiyacınız var, bunları referans kitaplarında arayabilir veya çevrimiçi olarak, örneğin webelements.com'da arayabilirsiniz. Birincisi, her izotopun kütle atomu veya atomik kütlesidir. Daha fazla nötron içeren izotopların kütlesi daha fazladır.- Örneğin, gümüş izotop Ag-107, kütle atomuna sahiptir. 106.90509 amu (kübik atom birimi). İzotop Ag-109, kütle ile biraz daha ağırdır. 108,90470.
- Belgelerin sonundaki ondalık sayı çifti biraz farklı olabilir. Kütleden sonra parantez içine herhangi bir sayı yazmayınız.

Her izotop için doğal hayatta kalma oranını yazın. Bu oran, elementin toplam atomlarının yüzdesi olarak izotop prevalansını gösterir. Bu bilgiyi aynı belgede üzerinde kübik bir atomla bulabilirsiniz. Tüm izotopların doğal sağkalımı% 100 olmalıdır (yuvarlama hatası nedeniyle biraz farklılık gösterebilir).- Ag-107 izotopu% 51.86 oranına sahiptir. Ag-109 izotopu,% 48.14 oranında daha az yaygındır. Bu, normal bir gümüş numunesinin% 51.86 Ag-107 ve% 48.14 Ag-109'a sahip olduğu anlamına gelir.
- Bu hayatta kalma oranı olmayan herhangi bir izotop ihmal edilir. Bu izotoplar yeryüzünde doğal olarak mevcut değildir.

İzotop yüzdesini ondalık sayıya dönüştürün. Bu oranı 100'e bölmek, ondalık sayı ile aynı değeri verecektir.- Yukarıdaki gümüş numunede izotop oranı 51,86 / 100 = 0,5186 ve 48,14 / 100 = 0,4814.
Ortalama kübik atomu bulun. Bir elementin ortalama kütle atomu, n izotoplar eşittir (Atomik Blokİzotop 1 * oranİzotop 1) + (atomik kütleİzotop 2 * oranİzotop 2) + ... + (kübik atomizotoplar n * oranizotoplar n. Bu, bir "ortalama kütle" örneğidir, yani izotopun hayatta kalma oranı ne kadar yüksekse, sonuç üzerindeki etkisi o kadar büyüktür. Bu formülün gümüş için nasıl uygulanacağı şu şekildedir:
- Orta kütleli atomAg = (kütle atomuAg-107 * oranAg-107) + (atomik kütleAg-109 * oranAg-109)
=(106,90509 * 0,5186) + (108,90470 * 0,4814)
= 55,4410 + 52,4267
= 107.8677 amu. - Sonuçları kontrol etmek için periyodik tabloda o öğeyi bulun. Ortalama kübik atom daima elementin kimyasal sembolünün altına yazılır.
- Orta kütleli atomAg = (kütle atomuAg-107 * oranAg-107) + (atomik kütleAg-109 * oranAg-109)
Bölüm 2/2: Sonuçları kullanma
Kütleyi atom numarasına dönüştür. Ortalama kütle atomu, o elementin tipik bir örneğindeki kütle ile atom sayısı arasındaki ilişkiyi gösterir. Bu, kimya laboratuvarlarında çok kullanışlıdır çünkü atomları doğru bir şekilde saymak neredeyse imkansızdır, ancak kütlelerin belirlenmesi kolaydır. Örneğin, bir gümüş numunesini tartabilir ve her 107.8677 amu için bir gümüş atomu olacağını bilirsiniz.
Molar kütleye dönüştür. Atomik kütle birimi çok küçüktür, bu nedenle kimyagerler genellikle kütle için gram birimini kullanırlar. Neyse ki bu kavramların tanımları var, bu yüzden dönüşüm kolay olmalı. G / mol sonucunu elde etmek için ortalama kütle atomunu 1 g / mol (molar kütle sabiti) ile çarpmanız yeterli. Örneğin 107,8677 gram gümüş, bir mol gümüş atomu içerir.
Ortalama moleküler kütleyi bulun. Bir molekül bir atomlar toplamı olduğundan, moleküler kütleyi bulmak için tüm atomların kütlesini toplayabilirsiniz. Ortalama bir kütle atomu kullandıysanız (belirli bir izotopun kütlesi yerine), sonuç, doğadaki bir numunenin ortalama moleküler kütlesi olacaktır. İşte bir örnek: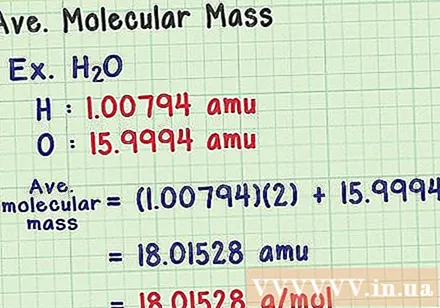
- Bir su molekülü, H kimyasal formülüne sahiptir.2O, iki hidrojen atomu (H) ve bir oksijen (O) atomu içerir.
- Hidrojenin ortalama kütle atomu 1,00794 amu'dur. Oksijenin ortalama atom kütlesi 15.9994 amu'dur.
- Yani H'nin ortalama moleküler kütlesi2O eşittir (1,00794) (2) + 15,9994 = 18,01528 amu, bu da 18,01528 g / mol'e eşdeğerdir.
Tavsiye
- Nispi atomik kütle kavramı bazen ortalama kütle atomuyla eşanlamlı olarak kullanılır. Küçük bir fark vardır çünkü atomik kütle nispeten birim değildir; bir karbon-12 atomuna göre kütlenin bir ölçüsüdür. Ortalama kübik atom hesaplamasında atomik kütle birimini kullandığınız sürece, bu iki değer aynıdır.
- Kübik atomdan sonra parantez içindeki sayı bize hatayı anlatır. Örneğin, kütle atomu 1.0173 (4), elementin normal atomunun yaklaşık 1.0173 ± 0.0004 kütle aralığına sahip olduğu anlamına gelir. İstenmediği takdirde bu numarayı almanıza gerek yoktur.
- Periyodik tabloda, aşağıdaki elementin ortalama kübik atomu, birkaç istisna dışında kendisinden öncekinden daha büyüktür. İşte sonuçlarınızı kontrol etmenin hızlı bir yolu.
- 1 atomik kütle birimi, bir karbon-12 atomunun kütlesinin 1 / 12'sidir.
- İzotop hayatta kalma oranları, yeryüzünde doğal olarak oluşan tipik örneklere göre hesaplanır. Meteorlar veya laboratuvarda üretilenler gibi doğal olarak oluşmayan maddeler farklı izotop oranlarına sahip olabilir, bu nedenle ortalama kütle atomu da farklıdır.
Uyarı
- Kütle atomları her zaman atomik kütle birimleri (amu veya u), bazen dalton (Da) olarak da yazılır. Bu sayıdan sonra değiştirmeden başka bir kütle birimi (kilogram gibi) asla yazmayın.
Neye ihtiyacın var
- Kalem
- Kağıt
- Dizüstü bilgisayar
- Doğadaki izotop hayatta kalma oranıyla ilgili veriler.
- İzotoplar için kütle atomik birim verileri.