Yazar:
Eric Farmer
Yaratılış Tarihi:
10 Mart 2021
Güncelleme Tarihi:
1 Temmuz 2024

İçerik
- adımlar
- Yöntem 1/2: Atomlardaki (izotop değil) nötron sayısının belirlenmesi
- Yöntem 2/2: İzotoplardaki Nötron Sayısının Belirlenmesi
- İpuçları
Aynı elementin atomlarında proton sayısı sabitken nötron sayısı değişebilir.Belirli bir atomun kaç nötron içerdiğini bilerek, bunun normal bir atom mu yoksa daha az veya daha fazla nötrona sahip olacak bir izotop mu olduğunu belirleyebilirsiniz. Bir atomdaki nötron sayısını belirlemek oldukça basittir. Bir atom veya izotoptaki nötron sayısını hesaplamak için yapmanız gereken tek şey talimatlarımızı takip etmek ve periyodik tabloyu elinizin altında tutmaktır.
adımlar
Yöntem 1/2: Atomlardaki (izotop değil) nötron sayısının belirlenmesi
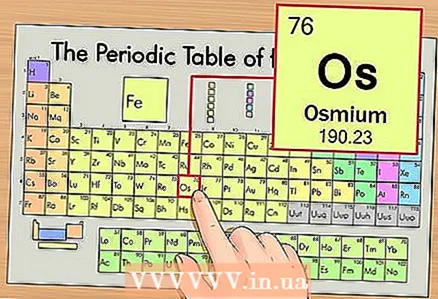 1 Periyodik tablodaki elementi bulun. Örnek olarak altıncı periyotta (üstten altıncı sıra) bulunan osmiyumu (Os) ele alacağız.
1 Periyodik tablodaki elementi bulun. Örnek olarak altıncı periyotta (üstten altıncı sıra) bulunan osmiyumu (Os) ele alacağız.  2 Elementin atom numarasını bulunuz. Bu, kural olarak, bir elementin hücresindeki en dikkat çekici sayıdır ve genellikle sembolünün üzerinde bulunur (örneğimizde kullandığımız periyodik tablonun versiyonunda başka sayı yoktur). Atom numarası, o elementin bir atomundaki proton sayısıdır. Osmiyum için bu sayı 76'dır, yani bir osmiyum atomunda 76 proton vardır.
2 Elementin atom numarasını bulunuz. Bu, kural olarak, bir elementin hücresindeki en dikkat çekici sayıdır ve genellikle sembolünün üzerinde bulunur (örneğimizde kullandığımız periyodik tablonun versiyonunda başka sayı yoktur). Atom numarası, o elementin bir atomundaki proton sayısıdır. Osmiyum için bu sayı 76'dır, yani bir osmiyum atomunda 76 proton vardır. - Proton sayısı değişmez ve bir elementi element yapan da budur.
 3 Bir elementin atom kütlesini bulun. Bu numara genellikle eleman sembolünün altında bulunur. Lütfen örneğimizdeki periyodik tablo versiyonunda atom kütlesinin verilmediğini unutmayın (bu her zaman böyle değildir; periyodik tablonun birçok versiyonunda atom kütlesi belirtilir). Osmiyumun atom kütlesi 190.23'tür.
3 Bir elementin atom kütlesini bulun. Bu numara genellikle eleman sembolünün altında bulunur. Lütfen örneğimizdeki periyodik tablo versiyonunda atom kütlesinin verilmediğini unutmayın (bu her zaman böyle değildir; periyodik tablonun birçok versiyonunda atom kütlesi belirtilir). Osmiyumun atom kütlesi 190.23'tür.  4 Atom kütlesini en yakın tam sayıya yuvarlayın. Örneğimizde 190.23, 190'a yuvarlanmıştır.
4 Atom kütlesini en yakın tam sayıya yuvarlayın. Örneğimizde 190.23, 190'a yuvarlanmıştır. - Atom kütlesi, belirli bir elementin ortalama izotop sayısıdır, genellikle bir tamsayı olarak ifade edilmez.
 5 Atom numarasını atom kütlesinden çıkarın. Atom kütlesinin mutlak kısmını protonlar ve nötronlar oluşturduğundan, atom kütlesinden proton sayısını (yani, proton sayısına eşit olan atom numarasını) çıkarmak, atomdaki nötron sayısını verir. Ondalık noktadan sonraki sayılar, bir atomdaki çok küçük elektron kütlesini ifade eder. Örneğimizde: 190 (atom ağırlığı) - 76 (proton sayısı) = 114 (nötron sayısı).
5 Atom numarasını atom kütlesinden çıkarın. Atom kütlesinin mutlak kısmını protonlar ve nötronlar oluşturduğundan, atom kütlesinden proton sayısını (yani, proton sayısına eşit olan atom numarasını) çıkarmak, atomdaki nötron sayısını verir. Ondalık noktadan sonraki sayılar, bir atomdaki çok küçük elektron kütlesini ifade eder. Örneğimizde: 190 (atom ağırlığı) - 76 (proton sayısı) = 114 (nötron sayısı). 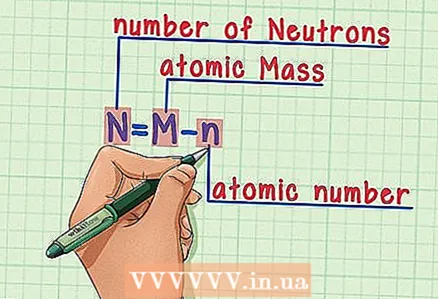 6 Formülü hatırla. Gelecekteki nötron sayısını bulmak için şu formülü kullanın:
6 Formülü hatırla. Gelecekteki nötron sayısını bulmak için şu formülü kullanın: - N = M - n
- N = nötron sayısı
- M = atom kütlesi
- n = atom numarası
- N = M - n
Yöntem 2/2: İzotoplardaki Nötron Sayısının Belirlenmesi
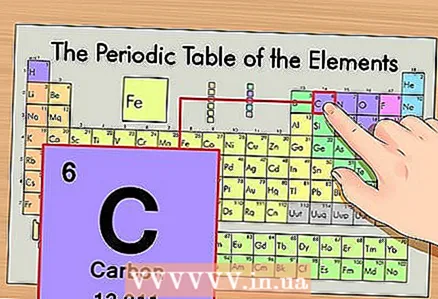 1 Periyodik tablodaki elementi bulun. Örnek olarak, karbon 14C izotopunu ele alacağız. İzotopik olmayan karbon 14C sadece karbon C olduğundan, periyodik tablodaki karbonu bulun (ikinci periyot veya üstten ikinci sıra).
1 Periyodik tablodaki elementi bulun. Örnek olarak, karbon 14C izotopunu ele alacağız. İzotopik olmayan karbon 14C sadece karbon C olduğundan, periyodik tablodaki karbonu bulun (ikinci periyot veya üstten ikinci sıra). 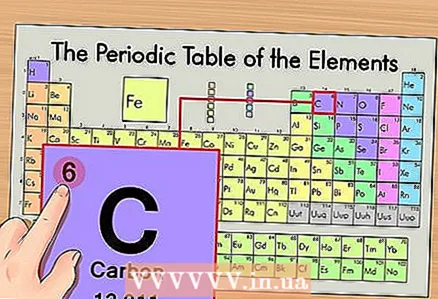 2 Elementin atom numarasını bulunuz. Bu, kural olarak, bir elementin hücresindeki en dikkat çekici sayıdır ve genellikle sembolünün üzerinde bulunur (örneğimizde kullandığımız periyodik tablonun versiyonunda başka sayı yoktur). Atom numarası, o elementin bir atomundaki proton sayısıdır. Karbon 6 numaradır, yani bir karbonun altı protonu vardır.
2 Elementin atom numarasını bulunuz. Bu, kural olarak, bir elementin hücresindeki en dikkat çekici sayıdır ve genellikle sembolünün üzerinde bulunur (örneğimizde kullandığımız periyodik tablonun versiyonunda başka sayı yoktur). Atom numarası, o elementin bir atomundaki proton sayısıdır. Karbon 6 numaradır, yani bir karbonun altı protonu vardır. 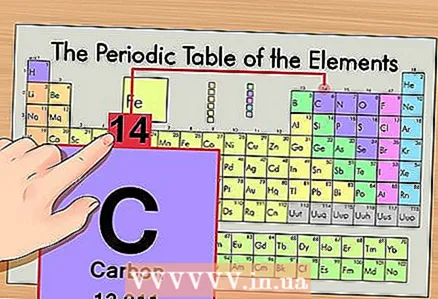 3 Atom kütlesini bulun. İzotoplar söz konusu olduğunda, atom kütlelerine göre adlandırıldıkları için bunu yapmak çok kolaydır. Bizim durumumuzda, karbon 14C'nin atom kütlesi 14'tür. Şimdi izotopun atom kütlesini biliyoruz; müteakip hesaplama işlemi, atomlardaki (izotop değil) nötron sayısını belirlemekle aynıdır.
3 Atom kütlesini bulun. İzotoplar söz konusu olduğunda, atom kütlelerine göre adlandırıldıkları için bunu yapmak çok kolaydır. Bizim durumumuzda, karbon 14C'nin atom kütlesi 14'tür. Şimdi izotopun atom kütlesini biliyoruz; müteakip hesaplama işlemi, atomlardaki (izotop değil) nötron sayısını belirlemekle aynıdır.  4 Atom numarasını atom kütlesinden çıkarın. Atom kütlesinin mutlak kısmını protonlar ve nötronlar oluşturduğundan, atom kütlesinden proton sayısını (yani, proton sayısına eşit olan atom numarasını) çıkarmak, atomdaki nötron sayısını verir. Örneğimizde: 14 (atom kütlesi) - 6 (proton sayısı) = 8 (nötron sayısı).
4 Atom numarasını atom kütlesinden çıkarın. Atom kütlesinin mutlak kısmını protonlar ve nötronlar oluşturduğundan, atom kütlesinden proton sayısını (yani, proton sayısına eşit olan atom numarasını) çıkarmak, atomdaki nötron sayısını verir. Örneğimizde: 14 (atom kütlesi) - 6 (proton sayısı) = 8 (nötron sayısı). 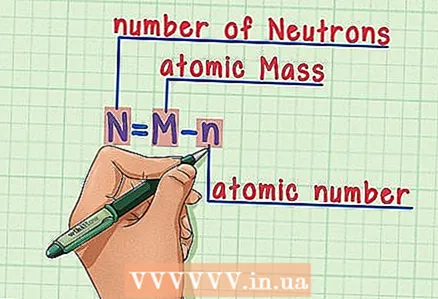 5 Formülü hatırla. Gelecekteki nötron sayısını bulmak için şu formülü kullanın:
5 Formülü hatırla. Gelecekteki nötron sayısını bulmak için şu formülü kullanın: - N = M - n
- N = nötron sayısı
- M = atom kütlesi
- n = atom numarası
- N = M - n
İpuçları
- Protonlar ve nötronlar elementlerin neredeyse mutlak kütlesini oluştururken, elektronlar ve diğer parçacıklar son derece önemsiz bir kütle oluşturur (bu kütle sıfır olma eğilimindedir).Bir proton, bir nötronla yaklaşık olarak aynı kütleye sahip olduğundan ve atom numarası proton sayısı olduğundan, proton sayısını toplam kütleden çıkarmanız yeterlidir.
- Osmiyum - oda sıcaklığında katı halde bulunan bir metal, adını Yunanca "osme" - koku kelimesinden almıştır.
- Periyodik tablodaki bir sayının ne anlama geldiğinden emin değilseniz, unutmayın: tablo genellikle 1 (hidrojen) ile başlayan ve soldan sağa doğru bir birim büyüyen bir atom numarası (yani proton sayısı) etrafında oluşturulur. , 118 (Oganesson) ile biten. Bunun nedeni, bir atomdaki proton sayısının elementin kendisini belirlemesidir ve böyle bir sayı, elementleri düzenlemenin en kolay yoludur (örneğin, 2 protonlu bir atom her zaman helyumdur, tıpkı 79 protonlu bir atomun her zaman altın olması gibi). ).



